2026年美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO GI)于1月8日至10日在美国旧金山举行。在本次大会上,复宏汉霖创新型抗PD-1单抗H药 汉斯状®在MSS/pMMR局部晚期结/直肠癌领域的两项新辅助研究结果以壁报形式正式发布,进一步彰显了H药在消化道肿瘤领域的治疗潜力。H药是全球首个且唯一胃癌围手术期III期注册研究成功的抗PD-1单抗,也是全球首个一线治疗小细胞肺癌的抗PD-1单抗,在肺癌和胃癌领域皆斩获全球突破性进展。
在消化道肿瘤治疗领域,H药除已获批食管鳞状细胞癌(ESCC)外,更是首个获得国家药品监督管理局(NMPA)药品审评中心(CDE)突破性疗法认定的胃癌围手术期治疗药物。作为全球首个胃癌围手术期以免疫单药取代术后辅助化疗的治疗方案,该适应症上市许可申请已获CDE受理并被纳入优先审评。此外,斯鲁利单抗联合贝伐珠单抗联合化疗一线治疗转移性结直肠癌(mCRC)的国际多中心临床研究(ASTRUM-015)III期研究已完成患者入组,有望填补一线免疫治疗non-MSI-H mCRC的临床空白。在本次ASCO GI大会上,H药公布了两项针对局晚期结/直肠癌的新辅助治疗IIT研究积极结果。数据显示,H药用于新辅助治疗有望提升局晚期高危结肠癌患者的根治性手术机会与长期生存率,同时也展现出为局晚期直肠癌患者提供免放疗治疗方案的潜力。
凭借其差异化的机制,H药在多种实体瘤的治疗中展现出独特优势,该药物不仅具备更强的PD-1内吞作用,可减少T细胞表面PD-1受体[1],实现快速、强效的免疫激活;还能减少PD-1对共刺激分子CD28的募集,从而更大程度保留CD28信号传导[2-4],增强下游AKT蛋白活性[5],促进T细胞持续活化。聚焦消化道肿瘤与肺癌,H药已获批用于治疗鳞状非小细胞肺癌(sqNSCLC)、广泛期小细胞肺癌(ES-SCLC)、ESCC和非鳞状非小细胞肺癌(nsNSCLC) 适应症,在中国、英国、德国、新加坡、印度等40多个国家获批上市,覆盖全球近半数人口。其关键性临床研究结果发表于JAMA、Nature Medicine、Cancer Cell和British Journal of Cancer等顶级学术期刊,并获得美国、欧盟、瑞士、韩国、墨西哥孤儿药资格认定。
此次ASCO GI大会上发布的两项研究数据结果如下:

论文题目:新辅助短程放疗联合 CAPOX 方案与 PD-1 抑制剂用于 MSS/pMMR 高危局部晚期结肠癌:一项随机、前瞻性、多中心 Ⅱ 期试验(TORCH-C)
试验设计:这是一项前瞻性、多中心、随机II期试验(NCT05732493)。总共120例LACC (T4/大体积N+M0,pMMR/MSS)患者将随机分为化疗组或放疗组。化疗组给予4个周期的CAPOX。放疗组接受5次25Gy的SCRT治疗,PD-1抑制剂(斯鲁利单抗)联合CAPOX治疗4个周期。放疗靶体积仅包括原发结肠肿瘤和肿大的淋巴结,没有选择性淋巴结照射。在新辅助治疗后,患者将评估根治性结肠切除术。主要终点是病理完全缓解(pCR)率。次要终点包括肿瘤降期,R0切除,3年无病生存期(DFS),3年总生存期(OS),3年局部无复发生存期和治疗相关毒性
结果:截至2025年8月31日,已有120名患者入组并随机分组。其中79例患者完成了新辅助治疗和手术(化疗组43例,放疗组36例)。79例患者均获得根治性切除,化疗组R0切除率为95.3%(41/43),放疗组R0切除率为97.2% (35/36)。化疗组pCR率(TRG 0)为11.6%(5/43),放疗组为47.2%(17/36)。完成新辅助治疗的患者中最常见的3-4级不良事件(AE)是血小板减少(15.3%,15/98),其中4级血小板减少5例。
结论:PD-1抑制剂、SCRT和化疗联合应用效果良好,可显著提高MSS/pMMR高危LACC患者的pCR率。该方案可能为实现R0切除和提高长期生存率提供新的治疗选择。
论文题目:新辅助化疗联合斯鲁利单抗用于 MSS/pMMR 局部晚期直肠癌(FIRM 研究):一项 Ⅱ 期临床试验
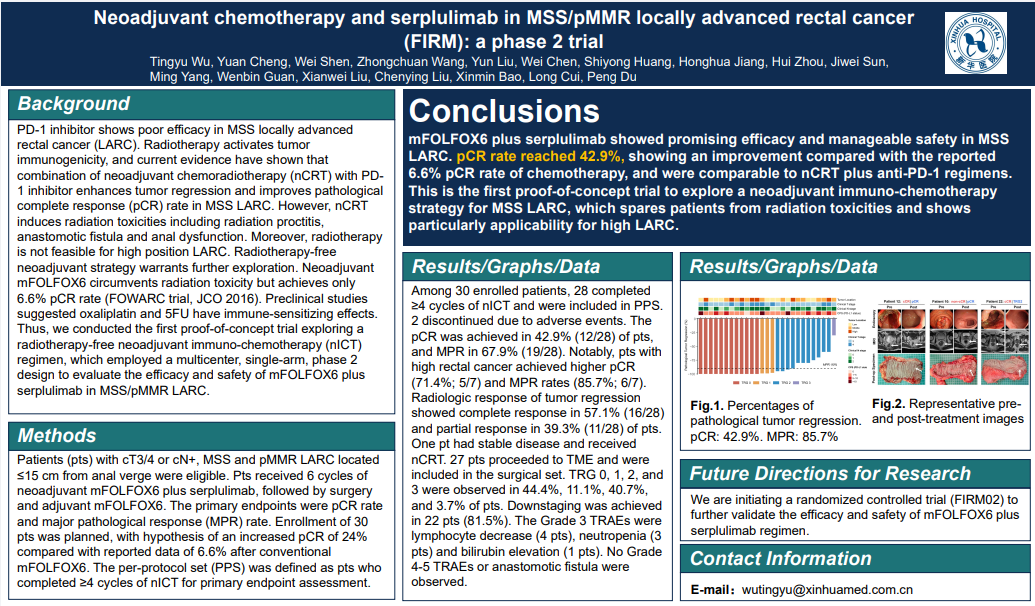
试验设计:入组cT3/4或cN+,距肛缘≤15 cm,MSS/pMMR的 LARC患者(pts),接受6个周期的新辅助mFOLFOX6和斯鲁利单抗,随后进行手术和辅助mFOLFOX6。主要终点为pCR率和主要病理反应(MPR)率
结果:在30例入组患者中,28例完成了≥4个nICT周期并纳入PPS。2例因不良事件停用。pCR是在42.9% (12/28), MPR 67.9%(19/28)。高位LARC(距肛缘10 cm,不适合nCRT)患者的pCR和MPR率分别为71.4%和85.7%
结论:mFOLFOX6联合斯鲁利单抗在MSS LARC中显示出良好的疗效和可管理的安全性。pCR率出乎意料地达到42.9%,与化疗报道的6.6% pCR率相比有所改善,与nCRT +抗pd -1方案相当。这是探索MSS LARC的nICT策略的第一个概念验证试验,该策略使患者免于放疗毒性,并特别适用于高位LARC。
参考文献
[1] Issafras H, et al. Structural basis of HLX10 PD-1 receptor recognition, a promising anti-PD-1 antibody clinical candidate for cancer immunotherapy. PLoS One. 2021;16(12):e0257972.
[2] Hui E, et al. T cell costimulatory receptor CD28 is a primary target for PD-1-mediated inhibition. Science. 2017;355(6332):1428-1433.
[3] Patsoukis N, et al. Interaction of SHP-2 SH2 domains with PD-1 ITSM induces PD-1 dimerization and SHP-2 activation. Commun Biol. 2020;3(1):128.
[4] Fenwick C, et al. Tumor suppression of novel anti-PD-1 antibodies mediated through CD28 costimulatory pathway. J Exp Med. 2019;216(7):1525-1541.
[5] Primavera E, et al. Computer-Aided Identification of Kinase-Targeted Small Molecules for Cancer: A Review on AKT Protein. Pharmaceuticals (Basel). 2023;16(7):993.


