2026年美國臨床腫瘤學會胃腸道腫瘤研討會(ASCO GI)於1月8日至10日在美國三藩市舉行。在本次大會上,復宏漢霖創新型抗PD-1單抗H藥 漢斯狀®在MSS/pMMR局部晚期結/直腸癌領域的兩項新輔助研究結果以壁報形式正式發佈,進一步彰顯了H藥在消化道腫瘤領域的治療潛力。H藥是全球首個且唯一胃癌圍手術期III期註冊研究成功的抗PD-1單抗,也是全球首個一線治療小細胞肺癌的抗PD-1單抗,在肺癌和胃癌領域皆斬獲全球突破性進展。
在消化道腫瘤治療領域,H藥除已獲批食管鱗狀細胞癌(ESCC)外,更是首個獲得國家藥品監督管理局(NMPA)藥品審評中心(CDE)突破性療法認定的胃癌圍手術期治療藥物。作為全球首個胃癌圍手術期以免疫單藥取代術後輔助化療的治療方案,該適應症上市許可申請已獲CDE受理並被納入優先審評。此外,斯魯利單抗聯合貝伐珠單抗聯合化療一線治療轉移性結直腸癌(mCRC)的國際多中心臨床研究(ASTRUM-015)III期研究已完成患者入組,有望填補一線免疫治療non-MSI-H mCRC的臨床空白。在本次ASCO GI大會上,H藥公佈了兩項針對局晚期結/直腸癌的新輔助治療IIT研究積極結果。數據顯示,H藥用於新輔助治療有望提升局晚期高危結腸癌患者的根治性手術機會與長期生存率,同時也展現出為局晚期直腸癌患者提供免放療治療方案的潛力。
憑藉其差異化的機制,H藥在多種實體瘤的治療中展現出獨特優勢,該藥物不僅具備更強的PD-1內吞作用,可減少T細胞表面PD-1受體[1],實現快速、強效的免疫激活;還能減少PD-1對共刺激分子CD28的募集,從而更大程度保留CD28信號傳導[2-4],增強下游AKT蛋白活性[5],促進T細胞持續活化。聚焦消化道腫瘤與肺癌,H藥已獲批用於治療鱗狀非小細胞肺癌(sqNSCLC)、廣泛期小細胞肺癌(ES-SCLC)、ESCC和非鱗狀非小細胞肺癌(nsNSCLC) 適應症,在中國、英國、德國、新加坡、印度等40多個國家獲批上市,覆蓋全球近半數人口。其關鍵性臨床研究結果發表於JAMA、Nature Medicine、Cancer Cell和British Journal of Cancer等頂級學術期刊,並獲得美國、歐盟、瑞士、韓國、墨西哥孤兒藥資格認定。
此次ASCO GI大會上發佈的兩項研究數據結果如下:

論文題目:新輔助短程放療聯合 CAPOX 方案與 PD-1 抑制劑用於 MSS/pMMR 高危局部晚期結腸癌:一項隨機、前瞻性、多中心 Ⅱ 期試驗(TORCH-C)
試驗設計:這是一項前瞻性、多中心、隨機II期試驗(NCT05732493)。總共120例LACC (T4/大體積N+M0,pMMR/MSS)患者將隨機分為化療組或放療組。化療組給予4個周期的CAPOX。放療組接受5次25Gy的SCRT治療,PD-1抑制劑(斯魯利單抗)聯合CAPOX治療4個周期。放療靶體積僅包括原髮結腸腫瘤和腫大的淋巴結,沒有選擇性淋巴結照射。在新輔助治療後,患者將評估根治性結腸切除術。主要終點是病理完全緩解(pCR)率。次要終點包括腫瘤降期,R0切除,3年無病生存期(DFS),3年總生存期(OS),3年局部無復發生存期和治療相關毒性
結果:截至2025年8月31日,已有120名患者入組並隨機分組。其中79例患者完成了新輔助治療和手術(化療組43例,放療組36例)。79例患者均獲得根治性切除,化療組R0切除率為95.3%(41/43),放療組R0切除率為97.2% (35/36)。化療組pCR率(TRG 0)為11.6%(5/43),放療組為47.2%(17/36)。完成新輔助治療的患者中最常見的3-4級不良事件(AE)是血小板減少(15.3%,15/98),其中4級血小板減少5例。
結論:PD-1抑制劑、SCRT和化療聯合應用效果良好,可顯著提高MSS/pMMR高危LACC患者的pCR率。該方案可能為實現R0切除和提高長期生存率提供新的治療選擇。
論文題目:新輔助化療聯合斯魯利單抗用於 MSS/pMMR 局部晚期直腸癌(FIRM 研究):一項 Ⅱ 期臨床試驗
試驗設計:入組cT3/4或cN+,距肛緣≤15 cm,MSS/pMMR的 LARC患者(pts),接受6個周期的新輔助mFOLFOX6和斯魯利單抗,隨後進行手術和輔助mFOLFOX6。主要終點為pCR率和主要病理反應(MPR)率
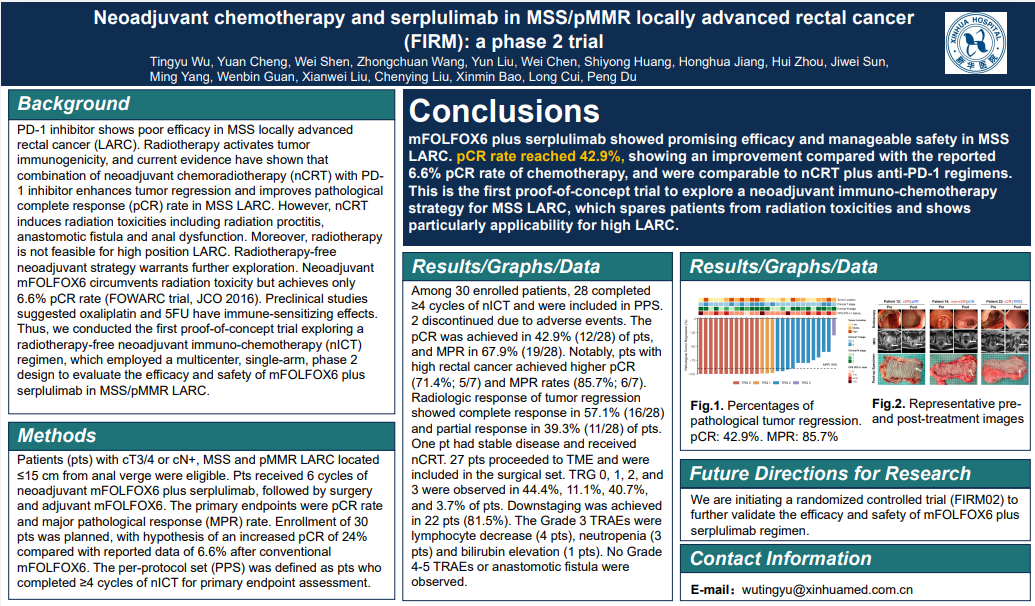
結果:在30例入組患者中,28例完成了≥4個nICT周期並納入PPS。2例因不良事件停用。pCR是在42.9% (12/28), MPR 67.9%(19/28)。高位LARC(距肛緣10 cm,不適合nCRT)患者的pCR和MPR率分別為71.4%和85.7%
結論:mFOLFOX6聯合斯魯利單抗在MSS LARC中顯示出良好的療效和可管理的安全性。pCR率出乎意料地達到42.9%,與化療報道的6.6% pCR率相比有所改善,與nCRT +抗pd -1方案相當。這是探索MSS LARC的nICT策略的第一個概念驗證試驗,該策略使患者免於放療毒性,並特別適用於高位LARC。
參考文獻
[1] Issafras H, et al. Structural basis of HLX10 PD-1 receptor recognition, a promising anti-PD-1 antibody clinical candidate for cancer immunotherapy. PLoS One. 2021;16(12):e0257972.
[2] Hui E, et al. T cell costimulatory receptor CD28 is a primary target for PD-1-mediated inhibition. Science. 2017;355(6332):1428-1433.
[3] Patsoukis N, et al. Interaction of SHP-2 SH2 domains with PD-1 ITSM induces PD-1 dimerization and SHP-2 activation. Commun Biol. 2020;3(1):128.
[4] Fenwick C, et al. Tumor suppression of novel anti-PD-1 antibodies mediated through CD28 costimulatory pathway. J Exp Med. 2019;216(7):1525-1541.
[5] Primavera E, et al. Computer-Aided Identification of Kinase-Targeted Small Molecules for Cancer: A Review on AKT Protein. Pharmaceuticals (Basel). 2023;16(7):993.
